Células de ingeniería para uso médico: aprender el idioma que usan las células para comunicarse entre sí
Share
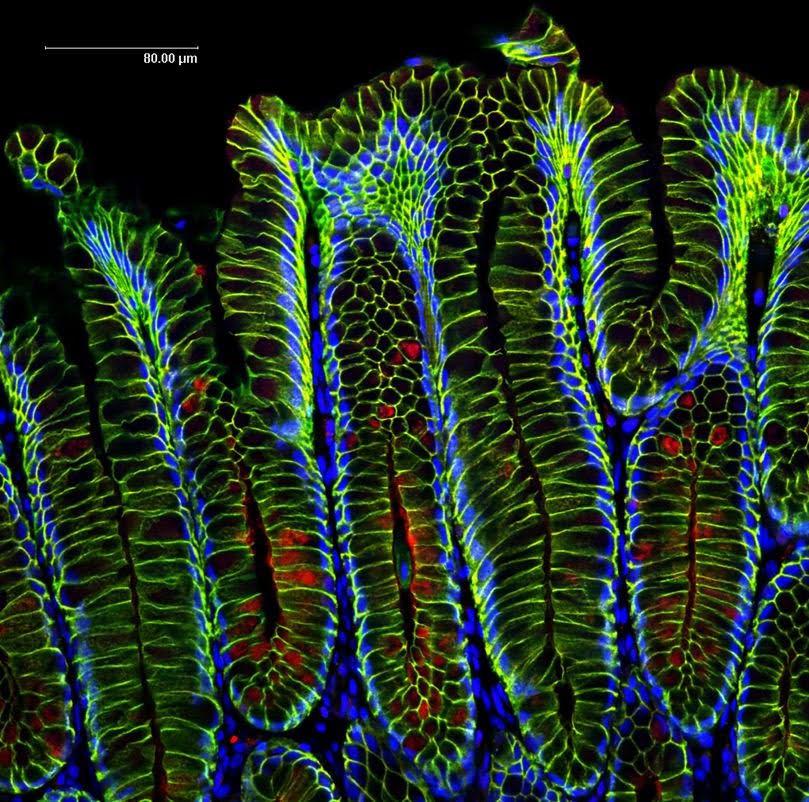
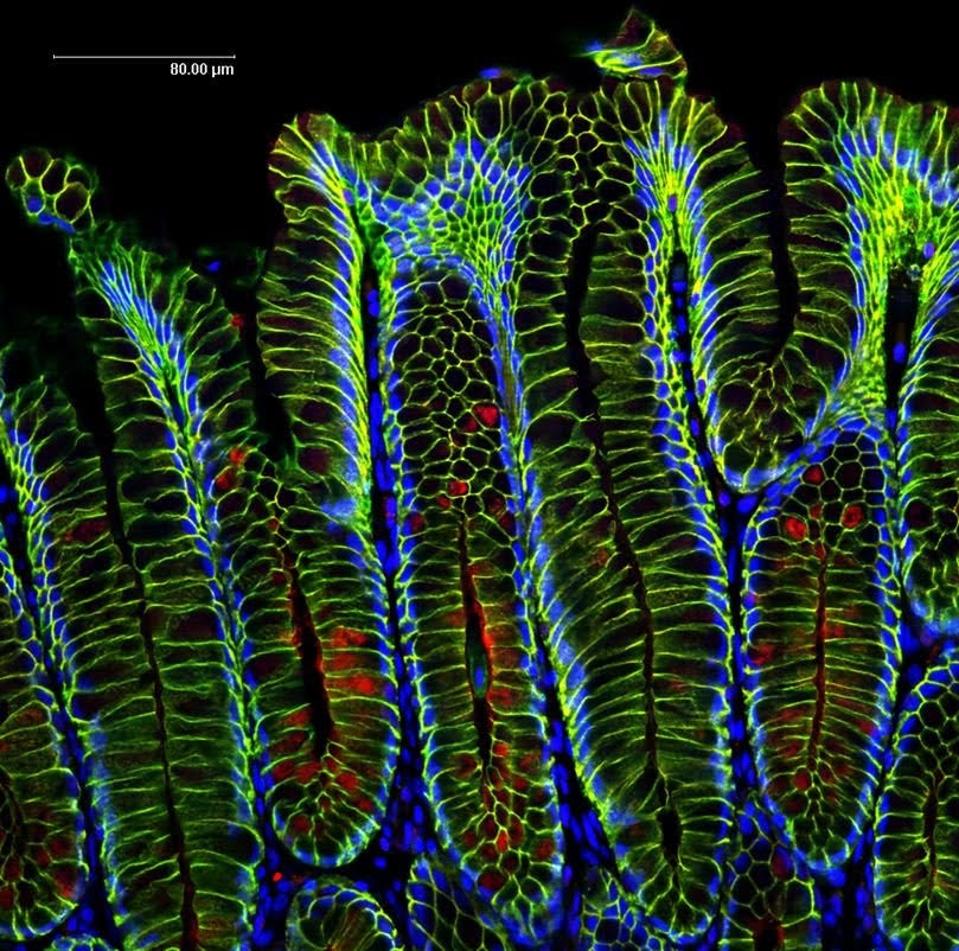
Células de la glándula estomacal
MPI para biología de infecciones
Las células son los componentes básicos de la vida. La forma en que las células reconocen a otras células y señales externas puede conducir a varios destinos biológicos, incluido el crecimiento celular, la muerte y la movilidad. Los investigadores buscan comprender la comunicación célula-célula, realizar ingeniería inversa y, en última instancia, esculpir interacciones celulares que superen las capacidades naturales. Aunque ya existen terapias celulares, el futuro de dicha terapia celular probablemente implicará una modificación más profunda de las células del paciente para tratar una gama de enfermedades y reparar tejidos.
En un artículo anterior, revisamos un estudio que sustituye modularmente la porción extracelular de una proteína para reconocer diferentes ligandos; esta proteína “reensamblada” transduce la misma vía de señal siempre que las porciones transmembrana e intracelular se mantengan intactas. Aquí, discutimos un documento que enfatiza la porción intracelular de la célula. Los investigadores de la Universidad de California en San Francisco recomponen teóricamente los dominios de señalización de las células CAR T y exploran los posibles impactos en la comunicación célula-célula.
Hacer un receptor de antígeno quimérico
Los receptores de antígenos quiméricos (CAR) requieren una modificación genética para expresar nuevos componentes sintéticos. La figura 1 ilustra las tres regiones principales de una célula T con CAR: el dominio de unión al antígeno, el dominio transmembrana y el dominio de señalización. Los científicos a menudo se fijan en el dominio de unión y lo adaptan para un objetivo terapéutico específico (por ejemplo, proteínas que se encuentran en las células cancerosas). Los investigadores aquí, sin embargo, se centran en la composición del dominio de señalización y su influencia en el rendimiento de las células CAR T.
Moléculas coestimuladoras
El dominio de señalización de una célula T con CAR generalmente contiene una molécula receptora de células T CD3ζ (TCR) y cualquier combinación de moléculas coestimuladoras. Las moléculas coestimuladoras contienen múltiples motivos de señal, o péptidos cortos que se unen a moléculas de señalización aguas abajo específicas. Estas moléculas influyen en la transducción de señales de las células T con diversos efectos. Dos ejemplos incluyen 4-1BB, que puede aumentar la memoria y la persistencia de las células T, y CD28, que se asocia con la destrucción eficaz de las células T pero con una menor persistencia de las células T.
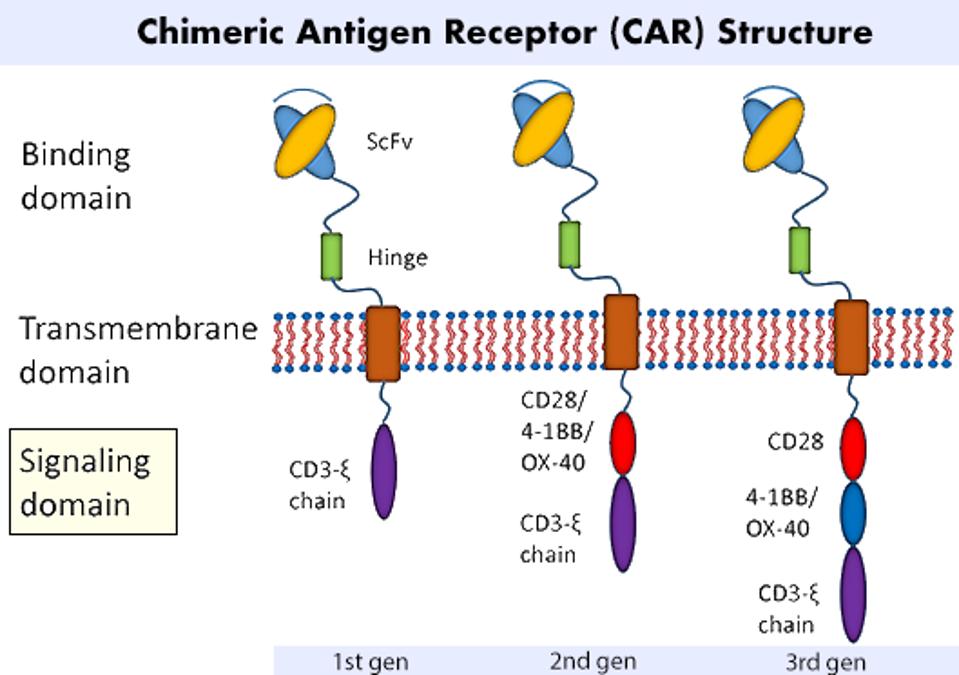
FIGURA 1: Un diseño de receptor de antígeno quimérico se puede dividir en tres regiones principales: un dominio de unión al antígeno… [+]; un dominio transmembrana; y un dominio de señalización. El dominio de señalización es más relevante para este estudio, ya que los investigadores investigan posibles combinaciones de moléculas coestimuladoras para mejorar el rendimiento y la capacidad de supervivencia de la célula T con CAR.
Liu et al.
Ampliando las posibilidades con el aprendizaje automático
Los investigadores del laboratorio de Wendell Lim buscaron encontrar reglas tácitas que rijan la señalización coestimuladora y, por lo tanto, optimizar las características de las células CAR T. Manejaron una biblioteca de motivos de señales sintéticas, aprendizaje automático y un enfoque conceptual único para descubrir combinaciones más allá de lo que ocurre naturalmente.
De las palabras a las oraciones y al lenguaje
Los investigadores buscaron proteínas de señalización naturales, extrajeron motivos de señal de ellas y ensamblaron sintéticamente combinaciones de motivos de señalización para formar programas de señalización únicos. Este enfoque puede conceptualizarse como una exploración de construcción de oraciones.
La figura 2 ilustra esta reorganización de varias "palabras" (motivos de señalización) en distintas "oraciones" o programas de señalización. Para comprender y predecir el "lenguaje" de estas combinaciones, el equipo utilizó algoritmos de aprendizaje automático llamados redes neuronales para detectar la "gramática" subyacente de los conjuntos de datos. Esto reveló la importancia del orden de las palabras, el significado de las palabras y las combinaciones de palabras en el producto final; de lo contrario, se reformularía como el impacto de la identidad, la función y la disposición del motivo de la señal en el fenotipo de las células T.
El equipo seleccionó una biblioteca de células T CAR anti-CD19 con una variedad de dominios coestimuladores. Cada célula contenía uno, dos o tres motivos de señal tomados de proteínas de señal naturales (ver Figura 2). El equipo insertó aleatoriamente 12 motivos de señales nativas junto con un motivo espaciador en las posiciones i, j y k para producir un total de 2379 configuraciones de motivos distintos, como se ve en la Figura 3.
A continuación, los investigadores seleccionaron subconjuntos aleatorios de la biblioteca para clasificar la citotoxicidad y la capacidad de proliferación (tallo) de las células T. Este proceso formó combinaciones únicas e inusuales, incluidas combinaciones comparables a la molécula coestimuladora 4-1BB (por ejemplo, M10-M1-M1-ζ).
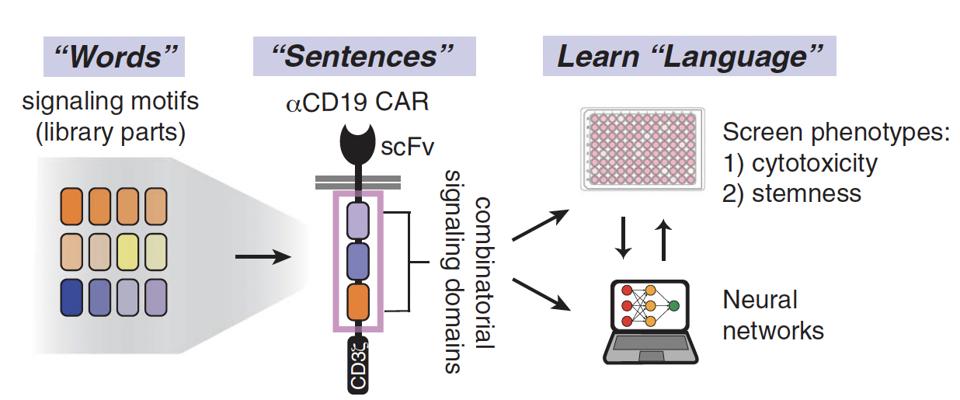
FIGURA 1: El procedimiento utilizado en este estudio se puede entender a través de una lente de "formación del lenguaje". … [+] Diferentes combinaciones de "palabras" o motivos de señalización de moléculas coestimuladoras crean "oraciones". Los algoritmos de aprendizaje automático y las redes neuronales descubren la "gramática" en las oraciones, es decir, las asociaciones entre la disposición de ciertos dominios de señalización y las características resultantes. Abreviaturas: scFv, fragmento variable (anticuerpo) monocatenario.
Daniels et al., 2022. 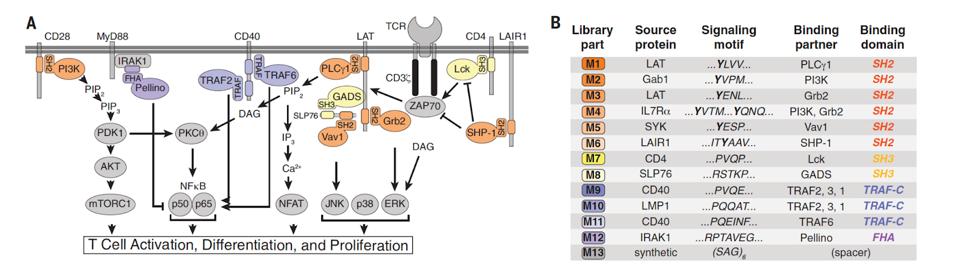
FIGURA 2: (A) Los investigadores buscaron proteínas de señalización naturales como la fosfolipasa C gamma 1… [+] (PLCg1) para crear su biblioteca de motivos de señales combinatorias. Estas proteínas desempeñan un papel en varias vías de señalización de células T, como la activación, la diferenciación y la proliferación. (B) La biblioteca contenía 12 motivos de señales nativas y un solo motivo espaciador para un total de 13 motivos.
Daniels et al., 2022. 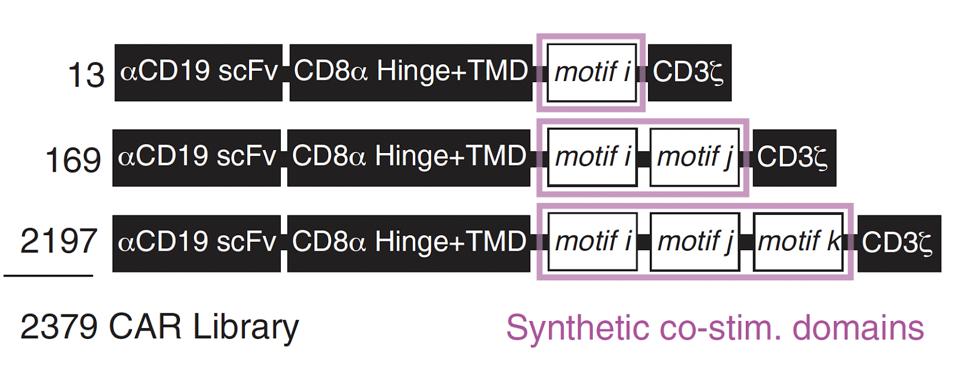
FIGURA 3: El equipo creó un total de 2379 combinaciones de motivos diferentes. Todas las células equiparon el… [+] mismo fragmento de anticuerpo anti-CD19 y dominio transmembrana/bisagra CD8α. El dominio de señalización contenía una molécula CD3ζ junto con una, dos o tres moléculas coestimuladoras sintéticas (resaltadas en rosa). Abreviaturas: scFv, fragmento variable (anticuerpo) monocatenario; TMD, dominio transmembrana.
Daniels et al., 2022.
Decodificando el “lenguaje” usando redes neuronales predictivas
Las secuencias de motivos de señalización poseían niveles variables de citotoxicidad y troncalidad, según el análisis experimental. Luego, el equipo aprovechó estos datos para comprender las reglas invisibles que rodean el diseño de moléculas coestimuladoras.
Una red neuronal artificial resultó crucial para esta investigación. Como se ve en la Figura 4, los datos se dividieron para entrenar o probar el algoritmo para predecir la citotoxicidad o la troncalidad de un receptor de antígeno quimérico. Este proceso aclaró varias asociaciones, como la capacidad de los dominios coestimuladores similares a 4-1BB para mejorar la citotoxicidad y la troncalidad.
Predicción exitosa con la molécula coestimuladora M1
¿Podría la red neuronal predecir con precisión el destino de una célula T con una combinación coestimuladora particular? El equipo probó las aguas agregando la molécula coestimuladora M1 a los dominios de señalización similares a 4-1BB frente a los similares a CD28. La red neuronal predijo que la adición de motivos M1 demostraría una mayor citotoxicidad y troncalidad en los dominios similares a 4-1BB sin tener ningún efecto en la contraparte similar a CD28.
En un modelo in vitro, las células CAR T con dominios similares a 4-1BB y motivos M1 mataron de manera efectiva las células tumorales y mantuvieron la progenitoridad de las células T; por otro lado, la adición de motivos M1 no provocó ningún cambio en los derivados similares a CD28. Esta predicción correcta también se tradujo en los resultados del modelo de ratón. Las células T CAR 4-1BB/M1 retrasaron el crecimiento de las células tumorales durante dos semanas más que las células T CAR 4-1BB solamente. Estas observaciones demuestran cómo se puede usar una red neuronal para pronosticar con precisión las características de las células T según los motivos de señalización sintéticos involucrados.
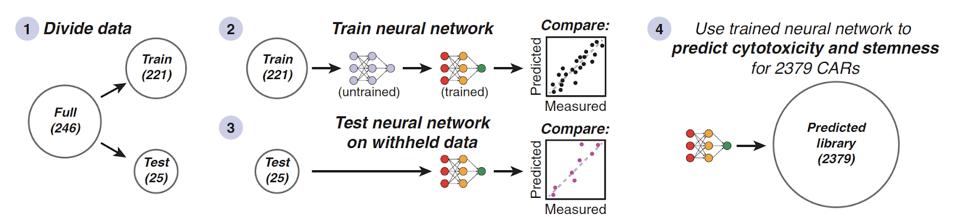
FIGURA 4: Las 248 combinaciones de moléculas coestimuladoras se usaron para entrenar o probar la red neuronal… [+].
Daniels et al., 2022.
Posibilidades de la terapia CAR T
Puede ser difícil predecir cómo un componente de receptor sintético influirá en las características de la célula resultante. Este estudio descifra parte de este misterio con bibliotecas de motivos de señales y aprendizaje automático. Mediante el análisis de las combinaciones de dominios coestimuladores de las células CAR T, el equipo creó una red neuronal que predice con éxito el fenotipo de las células T en función de las moléculas coestimuladoras presentes. Esto, a su vez, reveló reglas de señalización coestimuladora de CAR T que pueden usarse para diseñar mejores dominios de señalización sintéticos. Se podrían aplicar bibliotecas similares y análisis posteriores para mejorar otras regiones modulares de una célula CAR T.




