Прогрес у тканинній інженерії: контроль міжклітинної сигналізації


Клітинна адгезія залишається фундаментальним компонентом міжклітинної комунікації
ГЕТІ
Клітини є основною одиницею життя. У середньому людське тіло містить близько 30 трильйонів клітин із різними функціями та потенціалом. Комунікація між клітинами є центральною для здатності організму формувати тканини та органи, а також координувати важливі функції в організмі.
Зараз ми вивчаємо мову, яку клітини використовують для спілкування одна з одною в надії лікувати широкий спектр захворювань, а також відновлювати та регенерувати тканини. Недавня серія досліджень з’ясовує нові аспекти стільникового спілкування. Тут ми висвітлюємо дослідження, яке демонструє взаємозамінну природу між функцією рецепторів молекул клітинної адгезії та їх внутрішньоклітинними плазматичними областями.
Розуміння молекул клітинної адгезії (CAM)
Дослідники з лабораторії Wendell Lim досліджували взаємодію між клітинами, утворену молекулами клітинної адгезії. Молекули клітинної адгезії (CAM) є трансмембранними білками, які можуть опосередковувати взаємодію між клітинами. Ці молекули дозволяють клітині зв’язуватися або «прилипати» до сусідньої клітини за допомогою процесу, який називається клітинною адгезією. Організоване розташування клітин, з’єднаних цим клітинним клеєм, сприяє формуванню тканин, тоді як взаємодія може викликати каскад сигналів у клітині.
Розбиття компонентів
Щоб краще зрозуміти клітинну адгезію, важливо знати три основні області молекули клітинної адгезії. На малюнку 1 виділено кожну порцію білка.
Позаклітинний домен описує частину білка, яка знаходиться поза клітиною; ця частина білка зв'язується з іншими молекулами клітинної адгезії поблизу. Трансмембранний домен пронизує мембрану, а внутрішньоклітинний цитоплазматичний домен знаходиться всередині клітини.
Під час клітинної адгезії позаклітинний домен зв’язується з іншою молекулою клітинної адгезії. У відповідь трансмембранна область перебудовує структуру внутрішньоклітинного домену — процес, який називається алостеризмом — для активації внутрішньоклітинних сигнальних шляхів.
Малюнок 1 також ілюструє два основних типи молекул клітинної адгезії: кадгерини та інтегрини. Кадгерини повинні зв’язуватися з іншими молекулами кадгерину, щоб сприяти міжклітинному зв’язуванню. Навпаки, інтегрини зв’язуються з різними іншими молекулами адгезії, щоб прикріпити клітину до молекул, які знаходяться в позаклітинному матриксі (див. Малюнок 2). Кадгерини та інтегрини часто працюють поруч один з одним, створюючи багато форм стільникового зв’язку.
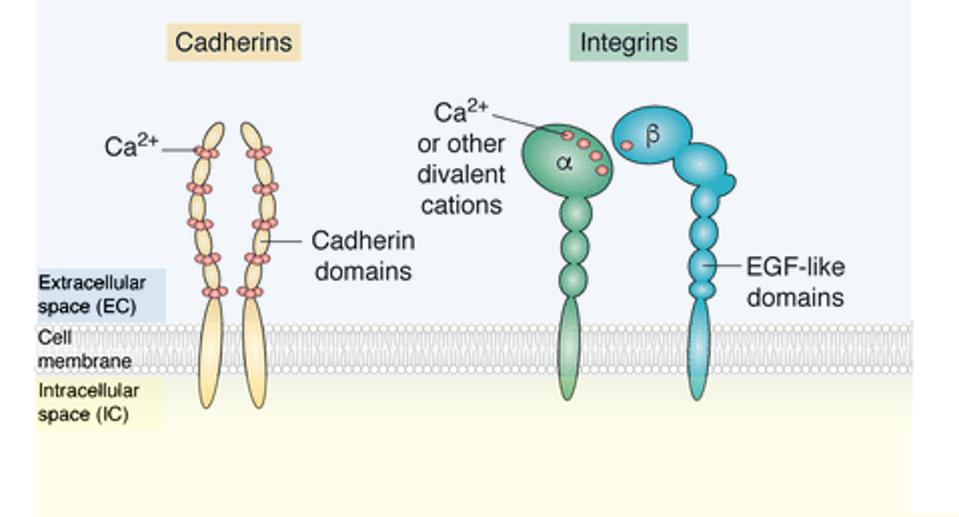
МАЛЮНОК 1. Існує багато типів молекул клітинної адгезії. Два приклади включають кадгерини та інтегрини. … [+] Функціонування кадгеринів залежить від іонів кальцію (Ca2+), тоді як інтегрини можуть використовувати різні ліганди. Важливо відзначити основні області молекул клітинної адгезії: позаклітинний домен, трансмембранний (клітинна мембрана) і внутрішньоклітинний домен. Скорочення: EGF-подібні домени, еволюційно консервативний білковий домен.
Янішевська та ін. 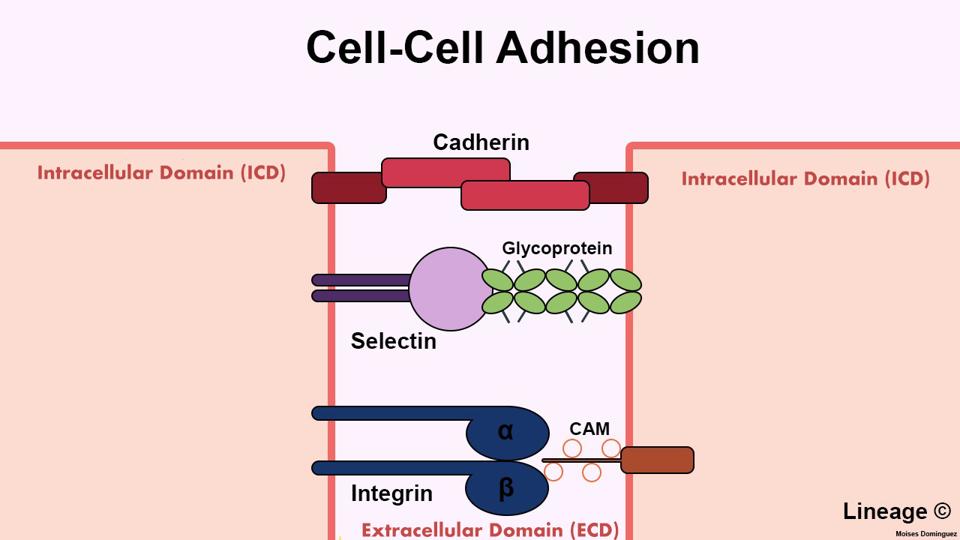
МАЛЮНОК 2. Молекули клітинної адгезії (CAM) зв’язуються різними способами. Кадгерини представляють сімейство … [+] молекул адгезії, які зв’язуються лише з кадгеринами, що знаходяться в інших клітинах. З іншого боку, інтегрини зв’язуються з різними типами молекул адгезії, щоб сприяти зв’язуванню клітини з позаклітинним матриксом. Хоча селектини не згадуються в цьому дослідженні, це молекули адгезії, які зв’язуються з молекулами цукру в інших клітинах.
Лі та Домінгес, 2019.
Синтетичні камери — як вони працюють?
У цьому дослідженні дослідники штучно сконструювали кілька типів синтетичних молекул клітинної адгезії, щоб краще зрозуміти основні правила та природу молекул клітинної адгезії в цілому. Маючи модульну конструкцію, команда замінила внутрішні компоненти — зокрема трансмембранного та внутрішньоклітинного матриксу — іншими компонентами позаклітинного матриксу, щоб отримати різні результати.
На першому етапі дослідження всі синтетичні молекули мали спільний зелений флуоресцентний білок, прикріплений до нанотіла α-зеленого флуоресцентного білка в позаклітинному матриксі. Внутрішня частина варіювалася між вісьмома різними внутрішньоклітинними областями, включаючи Е-кадгерин, інтегрин β1 і молекулу адгезії нейронних клітин 1. Команда також створила тетер — синтетичну молекулу лише з комбінацією зеленого флуоресцентного білка та без внутрішньоклітинного хвоста — для незалежно спостерігати вплив позаклітинного зв’язування. На рисунку 3 візуально порівнюється природне зчеплення, ремінь і синтетична адгезія.
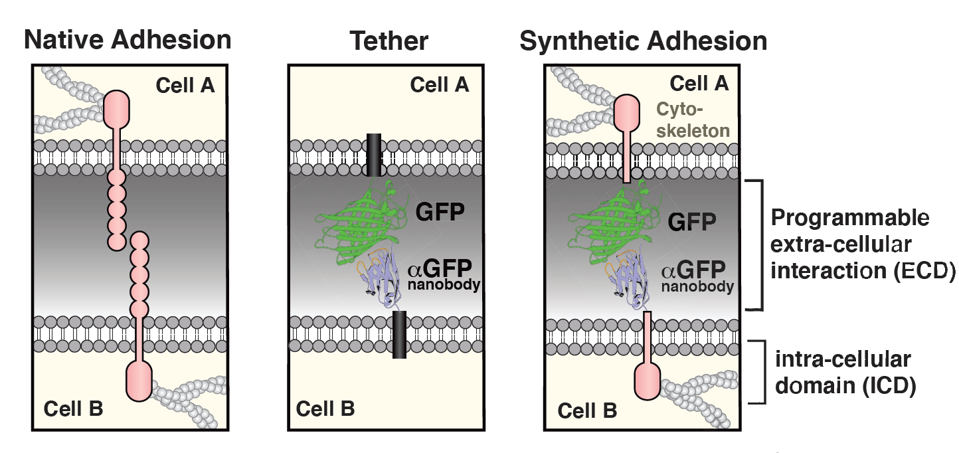
МАЛЮНОК 3: На відміну від нативної адгезії, молекули синтетичної клітинної адгезії можуть бути створені штучно з використанням … [+] різних додаткових і внутрішньоклітинних доменів. На цьому малюнку нанотіло зеленого флуоресцентного білка (GFP/αGFP) у позаклітинному домені поєднується з варіабельними молекулами в трансмембранних/внутрішньоклітинних доменах.
Стівенс та ін.
Порівняно з рідними CAM
Щоб вивчити ефективність нових молекул адгезії, команда проаналізувала інтерфейси зв’язування, створені під час використання синтетичних молекул адгезії для з’єднання клітин фібробластів мишей.
Синтетичні молекули клітинної адгезії працюють так само, як їхні природні комплементи. Деякі виготовлені молекули клітинної адгезії утворили нативні інтерфейси, незважаючи на наявність штучного позаклітинного домену. Інші молекули продемонстрували невеликий, але збагачений інтерфейс (див. Малюнок 4).
Тканинна інтеграція
Синтетичні молекули не тільки працюють порівнянно з нативними молекулами адгезії, але також успішно інтегруються в тканини, утворені нативними молекулами клітинної адгезії. Молекули природної клітинної адгезії (P-кадгерин) успішно взаємодіють із синтетичними молекулами клітинної адгезії, якщо їх вставити в тривимірну модель тканини.
Прийняття синтетичного до природного має значні наслідки при адаптації в багатоклітинному масштабі. Клітинна інженерія може змінити спосіб організації клітин і, таким чином, вплинути на побудову тканин.
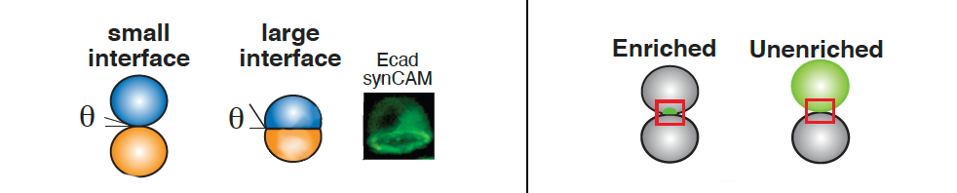
МАЛЮНОК 4: Команда спостерігала розмір (ліворуч) і збагачення (праворуч) інтерфейсу, утвореного їхніми … [+] синтетичними молекулами клітинної адгезії. Вони виявили, що синтетичні молекули утворюють або великі клітинні інтерфейси, схожі на рідні, або маленькі, але збагачені клітинні інтерфейси.
Стівенс та ін., 2023
Розуміння дизайну молекули синтетичної клітинної адгезії
Дослідники також виявили, які домени мають більший вплив на формування міжклітинних зв’язків. Вони виявили, що зменшення афінності зв’язування позаклітинного домену зменшує контактний кут — показник поверхневого натягу між клітинами і, отже, зв’язування, — але межа розділу залишається розширеною. Для порівняння, видалення внутрішньоклітинного домену повністю порушує інтерфейс. Ці спостереження демонструють, як позаклітинний домен самостійно визначає, з ким саме взаємодіє клітина, і як трансмембранний і внутрішньоклітинний механізм визначає характер інтерфейсу та цитоскелетну відповідь.
Майбутнє клітинної інженерії
Це дослідження поглиблює сучасне розуміння зв’язку між клітинами. Результати показують, що хоча позаклітинний домен розпізнає подразник, реакція клітини на подразник залежить від трансмембранної та цитоплазматичної областей білка; ті самі внутрішньоклітинні реакції виникають, коли цитоплазматична область прив'язана до гетерологічного позаклітинного домену.
Модульна природа цих синтетичних молекул і їхня здатність інтегруватися зі своїми нативними аналогами розширює поточні межі клітинної інженерії. Ці дослідження відкривають захоплюючу можливість для програмування нових клітинно-клітинних асоціацій для тканинної інженерії та контролю імунних і нервових клітинних взаємодій.

